J. Feld (Канада) и H.L.A. Janssen (Канада/Нидерланды)
Z. Abbas (Пакистан)
A. Elewaut (Бельгия)
P. Ferenci (Австрия)
V. Isakov (Россия)
A.G. Khan (Пакистан)
S.G. Lim (Сингапур)
S. Locarnini (Австралия)
S.K. Ono (Бразилия)
J. Sollano (Филиппины)
C.W. Spearman (Южная Африка)
C.T. Yeh (Тайвань)
M.F. Yuen (Гонконг)
A.W. LeMair (Нидерланды)
1. Вступление
Вирус гепатита В (HBV) вызывает острое и хроническое заболевание печени и эндемичен во многих регионах мира. Вирус передается через контакт с кровью или другими жидкостями тела от инфицированного человека.
- Инфекция обычно становится хронической, когда заражение происходит вертикально (от матери ребенку) или горизонтально маленькому ребенку (во время игры, бытовых контактов и т.д.).
- По контрасту, когда заражение происходит в подростковом/взрослом возрасте — чаще всего при половом контакте, через зараженные иглы, и, реже, при переливании крови и ее продуктов — инфекция обычно разрешается, если только индивидуум не иммуноскомпрометирован (например, заражен вирусом иммунодефицита человека).
- Важную роль в профилактике инфекции HBV имеет знание о том, как избежать поведения, связанного с риском заражения.
- Инфекция HBV является важным профессиональным фактором риска для медицинских работников.
- Безопасная и эффективная в 95% случаев, вакцина против HBV, позволяющая предотвратить возникновение новых эпизодов заражения, стала доступна с 1982 года.
Каждый человек с хронической инфекцией вируса гепатита В (ХГВ) представляет собой цель для профилактики дальнейшего распространения болезни. Очень важно посвятить необходимое время образованию пациентов и объяснить те риски, которые инфекция представляет для них самих и других людей.
- Вакцинация против HBV очень эффективна, и желательно ее всеобщее проведение в молодом возрасте – в странах с высокой эндемичностью предпочтительнее всего при рождении.
- Как минимум, вакцинация должна быть предложена всем лицам, находящимся в группе риска.
- У беременных женщин скрининг HBV должен проводиться до родов, поскольку это дает возможность предотвратить появление в следующем поколении хронически инфицированных людей.
Хотя у большинства пациентов с ХГВ не развиваются печеночные осложнения, у всех инфицированных имеется повышенный риск прогрессирующего фиброза печени, приводящего к циррозу и, в конечном итоге, к печеночной декомпенсации и/или гепатоцеллюлярной карциноме (ГЦК). К счастью, эффективное лечение может снизить риск развития осложнений, связанных с HBV.
1.1 Каскады ВГО
Данные Глобальные Практические Рекомендации ВГО включают в себя набор Каскадов, предназначенных обеспечить выбор вариантов диагностики и ведения гепатита В в зависимости от доступных ресурсов. Эти Каскады должны являться «глобальным» приложением, а не заменой «золотому стандарту» - Практическим Рекомендациям Европейской Ассоциации по Изучению Печени (EASL), Американской Ассоциации по Изучению Болезней Печени (AASLD), Азиатско-Тихоокеанской Ассоциации по Изучению Печени (APASL) и Национального Институт Помощи и Медицинского Мастерства (NICE) [1–4].
1.2 Эпидемиология и пути передачи гепатита В
Из множества заболеваний, вызываемых вирусами у людей, только немногие обладают такой же огромной глобальной значимостью, как вирус гепатита В [5]:
- Более 2 миллиардов человек на сегодняшний день имеют серологические доказательства прошлой или настоящей инфекции HBV.
- 250 миллионов хронически инфицированы и входят в группу риска развития заболеваний печени, связанных с HBV [6].
- Примерно у 15–40% хронически инфицированных пациентов в течение их жизни разовьется цирроз печени, прогрессирующий в печеночную недостаточность и/или ГЦК.
- Ежегодно отмечается более 4 миллионов клинических случаев острого гепатита В.
- Приблизительно 1 миллион человек ежегодно умирает от хронической инфекции HBV и ее осложнений: цирроза и первичного рака печени [7].
- Количество смертей от связанных с HBV болезней печени (2010) оценивается в 786,000 ежегодно [8].
Распространенность HBV значительно варьирует между разными мировыми регионами (Рис. 1). В литературе обычно указывается на различие между областями с высокой, средней, низкой и очень низкой эндемичностью.
- В высоко эндемичных областях [5], приблизительно 70–90% популяции заражается HBV в возрасте до 40 лет, и у 8–20% людей развивается хроническая инфекция с постоянным носительством вируса [9].
- Распространенность ХГВ варьирует от более 10% популяции в Юго- Восточной Азии, Китае, Амазонии и африканском сахарском регионе до менее чем 1% в Западной Европе и Северной Америке.
- В целом, примерно 45% населения земного шара живет в областях с высокой эндемичностью. С развитием глобализации многие люди с HBV мигрируют в области, в которых уровень ХГВ традиционно низок. Это обстоятельство легко может пройти незамеченным.
Рис. 1 Географическое распределение генотипов вируса гепатита В во всем мире (воспроизведено с разрешения [10,11]). Учитывая схемы миграции, распределение генотипов HBV при хроническом гепатите В может быстро изменяться, особенно в западных странах.
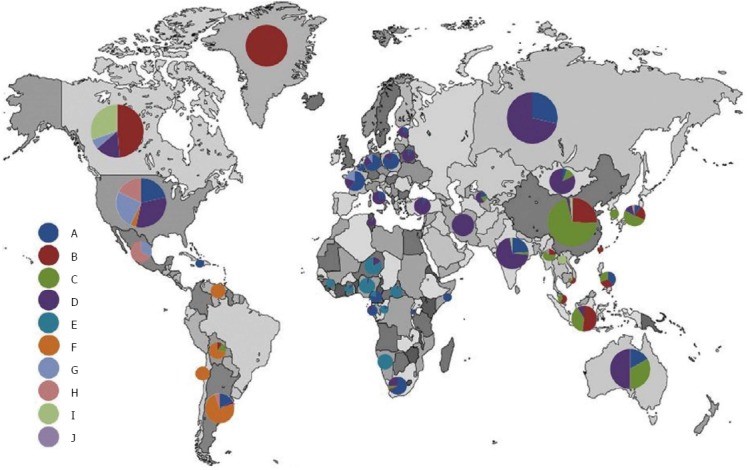
Замечания: Недавно опубликованные данные [12,13] показывают следующее распределение генотипов в России: генотип D, 85%; генотип A, 10.7%; генотип C, 3.2%; все другие генотипы, 1.1%. В Венесуэле, HBV генотип F наиболее часто встречается в общей популяции (также как в Колумбии и Перу) [14]; распространенность в городской популяции составляет приблизительно 80% [15], в то время как у индейцев она практически 100% [16].
Широкий диапазон цифр распространенности хронической инфекции HBV в основном связан с различиями в возрасте инфицирования.
- Вероятность того, что острая инфекция перейдет в хроническую составляет 70–90% при перинатальном (вертикальном) пути передачи, и 20–50% при заражении (горизонтальным путем) инфекцией в раннем детстве (в возрасте менее 5 лет).
- Вероятность развития ХГВ колеблется в диапазоне 1–3% у иммунокомпетентных взрослых с инфекцией, с более высокими показателями у лиц с иммуносупрессией.
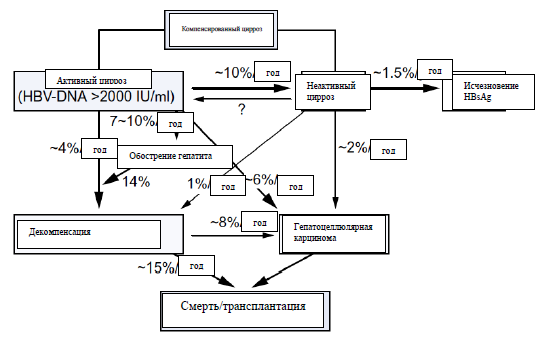
- Было идентифицировано восемь [17] (существует, возможно, до 10) генотипов вируса гепатита В (A–H), которые различаются в географическом распределении и в потенциале влияния на течение заболевания (Таблица 1). Распространенность генотипов HBV в различных регионах сильно зависит от схем миграции населения.
Таблица 1 Географическое распределение генотипов и субгенотипов инфекции гепатита В [10]
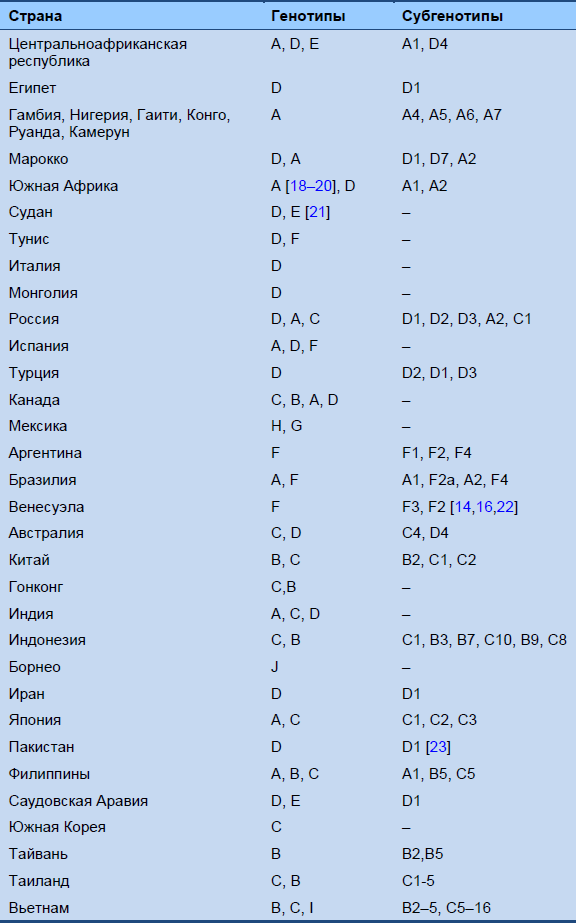
У все большего количества пациентов с хронической инфекцией развиваются варианты HBV, которые не экспрессируют или экспрессируют в малых количествах е антиген гепатита В (HBeAg); эта HBeAg-негативная форма гепатита В может потребовать проведения длительной терапии для уменьшения вероятности прогрессирования. При прекращении лечения у пациентов возникают рецидивы заболевания. Определяется различие между мутацией прекоровой зоны, при которой stop мутация в прекоровом гене полностью останавливает продукцию HBeAg, и мутацией основного корового промотора (ОКП), которая влияет на промотор и, следовательно, снижает, но не прекращает, продукцию HBeAg. Распространенность прекоровых мутаций наиболее высока в Средиземноморских странах, где также наиболее часто встречается генотип D, в то время как мутации корового промотера в основном отмечаются при генотипе C (в Восточной и Юго-Восточной Азии).
2. Клиническое течение инфекции HBV
Исход инфекции HBV в основном зависит от взаимодействия хозяина и вируса, опосредованном адаптивным иммунным ответом. Ответ вирусоспецифических Т-клеток – это один из ключевых факторов в патогенезе инфекции HBV. Варианты вирусов могут оказывать влияние на течение и исход заболевания. Эффект факторов хозяина на прогрессирование болезни плохо понимаем. Только очень редко (когда имеется глубокая иммунная супрессия) вирус гепатита В, вероятно, становится непосредственно цитопатичным.
2.1 Естественная история
Клиническое течение инфекции HBV разнообразно и включает острую (саморазрешающуюся) инфекцию, фульминантную печеночную недостаточность, состояние неактивного носительства и хронический гепатит с возможностью прогрессирования в цирроз и ГЦК [24,25].
2.2 Хроническая инфекция HBV
Риск хронизации при острой инфекции HBV связан с возрастом при первичном инфицировании. Взрослые, ставшие хронически инфицированными в детстве, имеют 15–25%-ный риск умереть от цирроза печени, связанного с HBV или рака печени. Риск значительно выше у мужчин, чем у женщин [26].
Таблица 2 Риск хронизации и возраст при первичном инфицировании

Рис. 2 Последовательность серологических маркеров при острой инфекции гепатита В (воспроизведено с разрешения [27]). A, разрешение острой инфекции; B, прогрессирование в хроническую инфекцию.
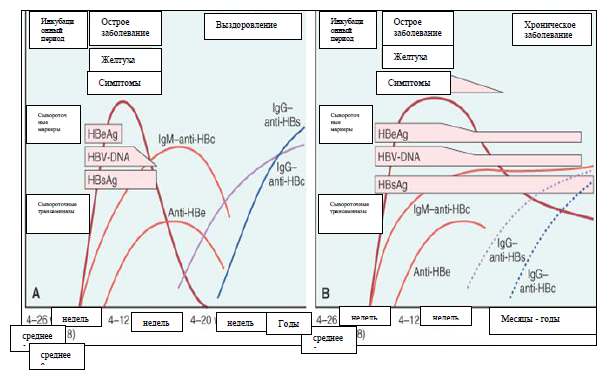
2.3 Фазы ХГВ
ХГВ – динамическое заболевание, изменяющееся в течение времени, вероятнее всего за счет взаимодействий между вирусом и иммунной системой хозяина. Ниже описаны пять – не обязательно последовательных – фаз, которые можно идентифицировать при хронической инфекции HBV.
- Иммунотолерантная фаза:
- Характеризуется высокими уровнями сывороточной HBV DNA, HBeAg позитивностью, нормальным уровнем аланин аминотрансферазы (АЛТ) и отсутствием некровоспаления в печени.
- У пациентов в этой фазе, прогрессирование заболевания минимально [28].
- В этой фазе пациенты высоко контагиозны.
- Иммунореактивная фаза (HBeAg-позитивный ХГВ):
- Эта фаза наступает у пациентов в разное время, в зависимости от возраста инфицирования.
- Иммунная системы активизируется и атакует инфицированные гепатоциты.
- Характеризуется высокой изменчивостью уровней HBV-DNA, но с прогрессирующим снижением, повышенным уровнем АЛТ и некровоспалением в печени (HBeAg-позитивный ХГВ).
- Длительная иммунореактивная фаза с многочисленными эпизодами повышения уровня АЛТ может привести к прогрессированию до фиброза печени, приводящему к циррозу.
- Фаза иммунного контроля (и состояния неактивного носительства):
- Переход в эту фазу, как результат иммуноактивной фазы, отмечается сероконверсией от HBeAg до анти-HBe позитивности.
- Характеризуется низким (< 2000 МЕ/мл) или неопределяемым уровнем сывороточной HBV DNA, нормальным уровнем АЛТ и исчезновением некровоспаления в печени (состояние неактивного носительства).
- Фаза реактивации (HBeAg-негативный ХГВ):
- Несмотря на сероконверсию HBe, может происходить реактивация репликации HBV, из-за селекции HBeAg-дефективных HBV мутантов.
- Характеризуется позитивными уровнями анти-HBe антител, колеблющимися уровнями HBV DNA и АЛТ, и высоким риском прогрессирования в тяжелый фиброз печени (HBeAg-негативный ХГВ).
- Периодические эпизоды повышения АЛТ, чередующиеся нормализацией, создают сложности в определении различия между HBeAg- негативным ХГВ и неактивным заболеванием. Следовательно, прежде чем признать пациента с нормальной АЛТ и низким уровнем HBV DNA неактивным носителем, необходимо проводить динамическое наблюдение.
- Появляющиеся доказательства позволяют предположить, что низкий титр HBV DNA (< 2000 МЕ/мл) в комбинации с низким титром поверхностного антигена гепатита В (HBsAg) (< 1000 МЕ/мл) может помочь в выявлении неактивных носителей, в частности с инфекцией генотипом D [29].
- HBsAg-негативная фаза:
- После исчезновения HBsAg может персистировать репликация HBV на низком уровне, с определяемой HBV DNA в печени и, редко, в сыворотке [30].
- У пациентов с «оккультной» инфекцией HBV было выявлено сохранение эффективного иммунологического контроля HBV [31].
- Выраженная иммуносупрессия может приводить к реактивации HBV, с повторным появлением HBsAg, известная как «обратная сероконверсия».
Рис. 3 Маркеры и естественная история инфекции хронического гепатита В (воспроизведено с разрешения [27]).
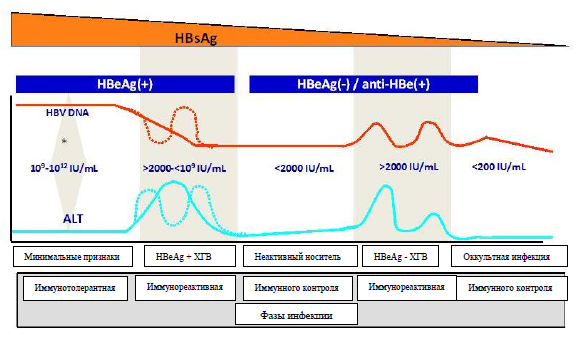
2.4 Прогрессирование ХГВ
ХГВ имеет очень изменчивое течение - от немой субклинической инфекции до персистирующего гепатита с прогрессирующим фиброзом, ведущим к циррозу, печеночной недостаточности и/или раку печени. Детерминанты исхода заболевания не полностью понятны, но они включают взаимодействующие между собой факторы вируса, хозяина и окружающей среды (Table 3). Вирусные детерминанты прогноза имеют различное значение в зависимости от стадии заболевания. Например, титры сывороточной HBV DNA выше всего в иммунотолерантной фазе заболевания, несмотря на отсутствие печеночного некровоспаления или прогрессирующего фиброза во время этого периода. Напротив, при HBeAg-негативном ХГВ, чем выше уровень HBV DNA, тем больше риск прогрессирования болезни и развития ГЦК. Уровни прогрессирования в цирроз и ГЦК и связанные уровни смертности показаны на Рис. 4.
Таблица 3 Факторы, влияющие на исход заболевания при хроническом гепатите В
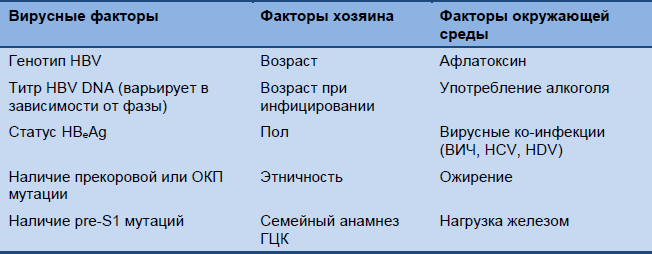
Рис. 4 Риск прогрессирования у пациентов с циррозом, вызванным HBV. Воспроизведено с разрешения Peng et al. (2012) [32], где можно найти детальную дискуссию о естественном течении цирроза, вызванного HBV и ГЦК.
3. Диагноз и наблюдение за гепатитом В
3.1 Каскад—острый гепатит B
Диагноз острого гепатита B основывается на выявлении HBsAg и анти-HBc (иммуноглобулин M).
- Во время первичной фазы болезни также присутствуют маркеры репликации HBV — HBeAg и HBV DNA.
- Выздоровление сопровождается исчезновением определяемой HBV DNA, сероконверсией HBeAg в анти-HBe, и последующим клиренсом HBsAg с сероконверсией в анти-HBs и появлением анти-HBc (IgG).
- Острой инфекция HBV считается в течение 3 месяцев с момента установления диагноза — хроническая инфекция HBV характеризуется сохранением HBsAg в плазме крови более 6 месяцев.
Редко, пациенты обращаются в период «окна», когда HBsAg уже стал негативным, а анти-HBs еще не позитивный. В таких обстоятельствах, которые чаще встречаются у пациентов с фульминантным гепатитом В, при котором вирусный клиренс происходит быстрее, иммуноглобулин М (IgM) анти-HBc остается единственным маркером острой инфекции HBV.
Каскад 1 Диагностические тесты при остром гепатите В

Дифференциальный диагноз HBsAg-позитивного острого гепатита включает обострения ХГВ, которые могут возникнуть в любое время у любого хронически инфицированного человека (в такие моменты может произойти реверсия к анти-HBc IgM). Острый гепатит может последовать за отменой иммуносупрессивной терапии или за счет суперинфекции у пациента хронической инфекцией гепатита В вирусом гепатита С и/или D, а также вирусом гепатита А. В форме острого гепатита может протекать наложившийся лекарственный или токсический гепатит у пациента с «немой» инфекцией ХГВ. Иногда провоцирующий фактор выявить не удается.
3.2 Разрешившаяся инфекция HBV
Ранее перенесенная инфекция HBV характеризуется наличием анти-HBs и IgG анти-HBc. Иногда анти-HBs становится неопределяемым через много лет. (Анти-HBs часто не определяется, если инфекция HBV была перенесена в детстве, что, кпримеру, наблюдается в сахарских областях Африки). В частности, хотя считается, что у этих пациентов имеется «разрешившаяся инфекция HBV», в их печени годами, а может быть и пожизненно, сохраняются следовые количества HBV DNA. Иммунный контроль предотвращает вирусную экспансию, но при тяжелой иммуносупрессии (например, при выраженной ко- инфекции вирусом иммунодефицита человека (ВИЧ), трансплантации костного мозга, при приеме ритуксимаба и т.д.), вновь может появиться HBsAg (обратная сероконверсия), или вирусная репликация может определяться в печени даже без повторного появления HBV DNA. Иммунитет к инфекции HBV после вакцинации характеризуется наличием только анти-HBs.
3.3 Хроническая инфекция HBV
Диагноз хронической инфекции HBV описывается как сохранение HBsAg более 6 месяцев.
- Сначала необходимо определить фазу инфекции у пациента: HBeAg-позитивную или HBeAg-негативную (Таблица 4).
- Должны быть проведены дополнительные тесты на маркеры репликации HBV — а именно, HBeAg и повторные измерения уровня сывороточной HBV DNA, в дополнение к АЛТ.
- Это частично определит необходимо ли проведение терапии HBV.
- Как HBeAg-позитивные, так и HBeAg-негативные пациенты, даже при нормальном уровне АЛТ в сыворотке крови (женщины < 20 МЕ/л и мужчины < 30 МЕ/л) и/или неопределяемой HBV DNA, все равно нуждаются в пожизненном наблюдении, поскольку состояние может со временем измениться, даже если пациенты остаются асимптоматичными.
- Пациенты с повышенным уровнем АЛТ, среди всех лиц с хроническим персистированием HBsAg, должны наблюдаться более тщательно, предпочтительно с проведением серий измерений уровня HBV DNA.
- Очень важно знать нижнюю границу определяемости HBV DNA при используемом методе, поскольку показатели, постоянно превышающие или равные 2000 МЕ/мл, заставляют обдумывать назначение противовирусной терапии.
- Решение о начале лечения зависит от множества факторов (т.е. не только от уровней HBV DNA и/или АЛТ). Если имеются подозрения о прогрессировании заболевания печени (на основании биопсии печени и результатов неинвазивных методов, таких как транзиентная эластография), так же рассматривается вопрос о назначении терапии.
- Для исключения суперинфекции гепатита С и гепатита D с другими вирусами необходимо проведение дополнительных исследований, особенно у пациентов с повышенным уровнем АЛТ, но с пониженной или неопределяемой HBV DNA.
- Также необходимо помнить о повреждении печени, вызванном приемом различных добавок, неалкогольном стеатогепатите (НАСГ) и перегрузки железом.
Таблица 4 Дифференциация фаз инфекции при ХГВ
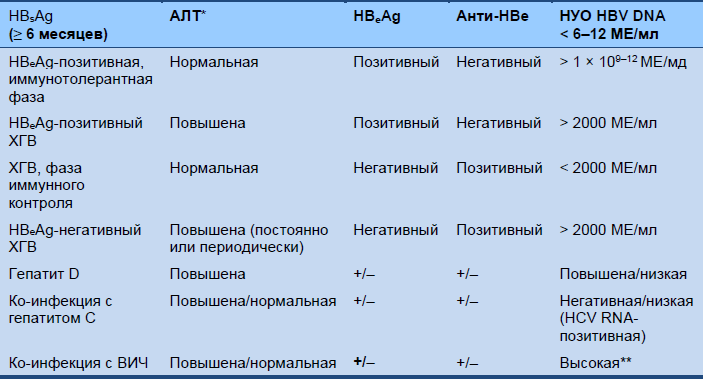
ХГВ, хронический гепатит B; HBeAg, е антиген гепатита В; HBsAg, поверхностный антиген гепатита В; HBV, вирус гепатита В; ВИЧ, вирус иммунодефицита человека; НУО, низший уровень определения.
*Нормальный показатель < 20 МЕ/л у женщин, < 30 МЕ/л у мужчин.
** Может быть вариабельной в зависимости от способа заражения и возраста при инфицировании HBV, ко-инфекции ВИЧ/HBV, и от подсчета CD4.
Показанием для начала терапии HBeAg-позитивного и HBeAg-негативного заболевания служат различные уровни HBV DNA в зависимости от генотипа, превалирующего в различных регионах. Как правило (поскольку генотипирование всех пациентов неосуществимо), для пациентов белой расы может использоваться уровень EASL: 2 × 103 МЕ/мл (и возраст > 30 лет); уровень APASL/AASLD может использоваться для азиатских пациентов: 2 × 104 МЕ/мл (и возраст > 40 лет).
3.4 Первичная оценка пациентов с хронической инфекцией HBV
Пациенты с впервые выявленным ХГВ, даже если у них отсутствует симптоматика, должны знать, что им предстоит длительное медицинское наблюдение за развитием хронического гепатита, цирроза печени и ГЦК с проведением серий клинических и лабораторных обследований. Врачу необходимо удостовериться в стадии ХГВ и решить вопрос о частоте необходимого динамического наблюдения.
- Хроническая инфекция HBV не обязательно сопровождается прогрессированием заболевания печени, требующим противовирусной терапии.
- Требуется точная оценка всех HBsAg-позитивных носителей для идентификации [33]:
- Фазы инфекции
- Степени воспаления в печени
- Стадии фиброза печени
- Конкурентных причин заболевания печени
- Необходимости лечения
- Наличия ко-факторов, повышающих риск прогрессирования в цирроз или ГЦК: ко-инфекции вирусом гепатита D (HDV), вирусом гепатита С (HCV) и ВИЧ; сопутствующих состояний, включающих алкоголизм, аутоиммунные заболевания, или метаболическую болезнь печени
Первичное обследование должно включать:
- Анамнез и физикальный осмотр, включая обследование кожи и брюшной полости.
- Маркеры инфекции HBV, включая: HBeAg/анти-HBe и HBV DNA для классификации фазы ХГВ, а также генотип HBV, если рассматривается вопрос об интерферонотерапии.
- Маркеры других вирусных инфекций, включая HCV и HDV, особенно если
АЛТ повышена, а уровень HBV DNA низкий или неопределяемый.
- Перед назначением оральной противовирусной терапии все пациенты должны быть скринированы на наличие вируса иммунодефицита человека (ВИЧ).
- Полная печеночная панель (АЛТ/АСТ для выявления активного воспаления; билирубин, протромбиновое время и альбумин - для проверки синтетической функции печени).
- Клинический анализ крови, особенно тромбоциты, которые служат суррогатным маркером портальной гипертензии.
- Ультразвуковое исследование брюшной полости как базовый скрининг на ГЦК. Анализ на альфа фетопротеин может проводиться в местностях с высокой эндемичностью HBV и слабо диагностируемой ГЦК, а также там, где доступ к ультразвуковому исследованию ограничен.
- Измерение фиброза печени с помощью серологического исследования, ФиброСкана (транзиентной эластографии) или биопсии печени.
Таблица 5 Факторы хозяина и вируса, связанные с прогрессированием хронического гепатита В

АЛТ, аланин аминотрансфераза; HBeAg, е антиген гепатита В; HBV, вирус гепатита В; ГЦК, гепатоцеллюлярная карцинома; HDV, вирус гепатита D; ВИЧ, вирус иммунодефицита человека; НАЖБП, неалкогольная жировая болезнь печени.
3.5 Оккультный HBV
Понятие оккультная инфекция HBV означает персистирование в ткани печени HBV DNA (и в некоторых случаях в сыворотке крови) у лиц, у которых в крови не определяется поверхностный антиген гепатита В (HBsAg)Э обычно с позитивным анти-HBc.
Оккультная инфекция HBV распространена во всем мире, но частота ее связана с общей распространенностью этого вируса в специфической географической области. Оккультная инфекция HBV передается при переливаниях крови и пересадках органов.
- Кровь и ее продукты должны проверяться на наличие HBsAg, анти-HBc и, в идеале, HBV DNA.
- Донорские органы с анти-HBc и/или анти-HBs предпочтительно использовать только для реципиентов с положительными тестами на анти- HBs или HBsAg.
Хотя истинная значимость оккультной инфекции HBV неизвестна, он может служить дополнительным фактором риска развития ГЦК у анти-HCV– позитивных пациентов и у ВИЧ-инфицированных лиц. Она также может быть связана с прогрессированием заболевания печени, вызванного отличными от HBV причинами.
3.6 Реактивация HBV
Репликация HBV контролируется иммунной системой хозяина. Иммуносупрессия любого вида может привести к потере иммунного контроля и последующей реактивацией HBV, которая способна вызвать разнообразные последствия, от субклинического повышения уровня HBV DNA до иктерической и даже фульминантной и/или фатальной печеночной недостаточности. Наиболее часто реактивация происходит при онкологической химиотерапии, но может развиться при и других видах иммуносупрессивной или иммуномодулирующей терапии (например, при таргетной иммунотерапии). Добавление системных кортикостероидов (СКС) к ингаляционным кортикостероидам повышает риск реактивации HBV, особенно когда СКС применяются длительно или в высоких дозах [35].
Превентивное лечение аналогами нуклеозидов/нуклеотидов рекомендовано HBsAg-позитивным пациентам, которым назначен курс противораковых или иммуносупрессивных препаратов. Лечение должно продолжаться в течение всего курса иммуносупрессии и 6–12 месяцев после него, с динамическим наблюдением за возможным обострением после отмены противовирусной терапии.
Реактивация может также произойти у HBsAg-негативных, но анти-HBc- позитивных пациентов (с оккультной HBV DNA или без нее), но для этого требуется более выраженная иммуносупрессия. Повторное появление HBsAg описывается как обратная сероконверсия. Риск, вероятно, возрастает при применении ритуксимаба или другой основанной на анти-CD20 химиотерапии, скорее всего за счет длительного истощения В клеток. HBV DNA может повыситься даже до того, как возникнет повторное появление HBsAg в сыворотке. Превентивное лечение аналогами нуклеозидов/нуклеотидов снижает риск реактивации HBV, но всем пациентам оно может не потребоваться [36]. Те больные, которые не получали превентивной терапии должны наблюдаться с проведением серийных исследований HBsAg, АЛТ и, возможно, HBV DNA. Противовирусное лечение таких пациентов начинается при повторном появлении HBsAg или возрастании уровня HBV DNA.
В целом:
- Перед началом химиотерапии или иммуносупрессивной/иммуномодуляторной терапии должно проводиться скринирование на HBsAg и анти-HBc, если необходимо.
- HBsAg-позитивные пациенты должны получать превентивную противовирусную терапию во время и в течение 6 – 12 месяцев после химиотерапии.
- Эффект превентивной терапии при реактивации оккультного HBV в настоящее время остается неясным.
- Пациентам, ранее перенесшим инфекцию HBV, что подтверждается позитивным анти-HBc с анти-HBs или без него, рекомендуется серийное мониторирование маркеров HBV во время и после иммуносупрессивной терапии.
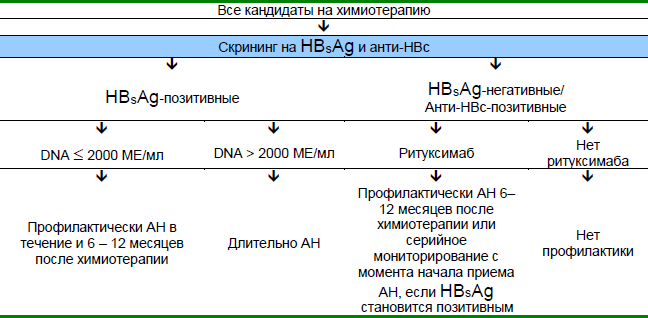
- Пациенты, получающие химиотерапию или иммуносупрессию, должны следовать практическим рекомендациям Американской Ассоциации по Изучению Болезней Печени (AASLD) и Азиатско-Тихоокеанской Ассоциации по Изучению Печени Liver (APASL) (Рис. 5).
Рис. 5 Алгоритм APASL для всех кандидатов на химиотерапию. АН, аналог нуклеозидов. Источник: Азиатско-Тихоокеанская Ассоциация по Изучению Печени.
3.7 Скрининг ГЦК
Целью является обнаружение опухолей размером менее 3 см в диаметре, предпочтительно менее 2 см, как потенциал для лечения. Скрининг на ГЦК показан всем пациентам с циррозом, как имеющим самый высокий риск развития опухоли. Тем не менее, в Африке и Юго-Восточной Азии, где заражение происходит в ранний период жизни, ГЦК может развиваться в нецирротической печени.
AASLD рекомендует наблюдение за возможным развитием ГЦК в следующих группах пациентов с ХГВ:
- Мужчины-азиаты старше 40 лет и женщины-азиатки старше 50 лет
- Все пациенты с циррозом, вне зависимости от возраста
- Пациенты с семейным анамнезом ГЦК в любом возрасте
- Африканцы старше 20 лет
- Любые пациенты с ко-инфекцией HBV/ВИЧ
Singal et al. показали, что в «реальных» клинических условиях комбинация ультразвукового исследования и определения альфа фетопротеина (АФП) является наиболее эффективной стратегией выявления ГЦК на ранней стадии. Чувствительность значительно повышается до 90%, с минимальной потерей специфичности (83%). Проведение только анализа на АФП может быть информативнее, чем проведение только ультразвукового исследования, поскольку последнее сильно зависит от мастерства и опыта врача [37].
Для носителей вируса гепатита В, не внесенных в список выше, риск развития ГЦК варьирует в зависимости от тяжести основного заболевания печени и воспалительной активности в печени в прошлом и на настоящий момент. Пациенты с высокой концентрацией HBV DNA и имеющейся воспалительной активностью в печени (судя по повышению уровня АЛТ) обладают повышенным риском развития ГЦК и подлежат наблюдению. Инфекция генотипом С и наличие ОКП и мутаций pre-S1 также связана с повышенным риском ГЦК.
4. Лечение ХГВ
До начала любой терапии, и оптимально при первых проявлениях заболевания, пациент должен быть обеспечен всей информацией о ХГВ и его лечении. Важные моменты:
- Динамическое клиническое течение ХГВ.
- Большинство случаев инфекции вначале протекают совершенно бессимптомно, даже когда заболевание серьезно.
- Необходимость регулярного пожизненного наблюдения.
- Возможная передача инфекции — семья и контакты должны проходить скрининг на HBV. Непривитым рекомендуется вакцинация против HBV, а HBsAg-позитивным лицам – консультация специалиста.
- Расчет времени начала лечения.
- Необходимость абсолютного согласия с потенциально долговременной терапией.
- Необходимость абсолютного согласия на динамическое наблюдение, как во время лечения, так и после его отмены.
- Важность воздержания от алкоголя и внимание к приему препаратов, обладающих гепатотоксичностью или опасностью для пациентов с выраженным заболеванием печени (например, НПВП).
- Лица, непривитые от гепатита А, должны получать две дозы вакцины с промежутком в 6 – 18 месяцев.
Эта информация должна быть объяснена и обсуждена с пациентом. Женщинам детородного возраста предпочтительно назначаются препараты, считающиеся безопасными при беременности, поскольку при назначении аналогов нуклеозидов/нуклеотидов их последующая отмена невозможна при сохранении HBeAg-позитивности. Пациент должен понять, что прекращение терапии может стимулировать развитие тяжелого гепатита, который редко, но приводит к фульминантной острой печеночной недостаточности даже при отсутствии цирроза.
Фаза ХГВ может быть определена на основании серологического и вирусологического профилей – каждый тип характеризуется определенным естественным течением, прогнозом и показаниями к лечению [1,2,38]
1 Иммунотолерантный носитель:
- Лечение не показано.
- Решающее значение имеет соответствующее динамическое наблюдение.
- Измерение АЛТ каждые 3–6 месяцев.
2 Неактивный носитель:
- Лечение не показано.
- Решающее значение имеет соответствующее динамическое наблюдение.
- Оценка уровней АЛТ и HBV DNA каждые 3 месяца в течение года, затем каждые 6 месяцев.
- Если уровень сывороточной HBV DNA < 2000 МЕ/мл и уровень HBsAg < 1000 МЕ/мл, вероятность реактивации заболевания низкая, и пациенту требуется более редкое наблюдение.
3 Активный ХГВ:
- HBeAg-позитивный ХГВ.
- HBeAg-негативный ХГВ.
Прогноз и ведение ХГВ сильно зависят от фазы заболевания и стадии фиброза печени, а, следовательно, риска развития цирроза. Динамическое наблюдение за ХГВ у носителей HBsAg включает:
- Продолжение динамического обследования.
- Оценку тяжести заболевания печени.
- Лабораторные тесты на воспаление (АЛТ), функцию печени (билирубин, альбумин, факторы коагуляции) и вирусную нагрузку (HBV DNA), если это доступно.
- Ультразвуковое исследование печени.
- Неинвазивные методы оценки фиброза (сывороточные панели, транзиентная эластография).
- Биопсия печени для определения степени некровоспаления и стадии фиброза. Также биопсия может помочь в исключении других сосуществующих причин болезни печени и в уточнении диагноза при дискордантности уровней АЛТ и HBV DNA.
Существующие в настоящее время стандарты для определения начала назначения лечения ХГВ показаны на Рисунках 6 и 7. Каскады включены для отражения вариантов в зависимости от ресурсов.
Рис. 6 Ведение хронической HBeAg-положительной инфекции. Наблюдение за возможным развитием гепатоцеллюлярной карциномы проводится по показаниям (в зависимости от возраста, пола, тяжести поражения печени и семейного анамнеза). Адаптировано из Lok and McMahon 2007 [39].
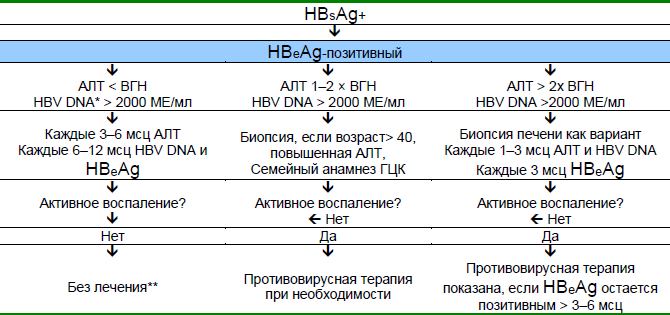
* У пациентов азиатского происхождения часто наблюдаются очень высокие уровни HBV DNA — в основном при перинатальном заражении. Неясно, должно ли таким пациентам назначаться противовирусное лечение АН. Уровень HBV DNA коррелирует с риском развития ГЦК во время наблюдения, но неясно уменьшает ли риск иммуносупрессия.
** Пациентам с циррозом и определяемой HBV DNA лечение должно назначаться вне зависимости от уровня АЛТ и HBV DNA.
Рис. 7 Ведение хронической HBeAg-негативной инфекции.
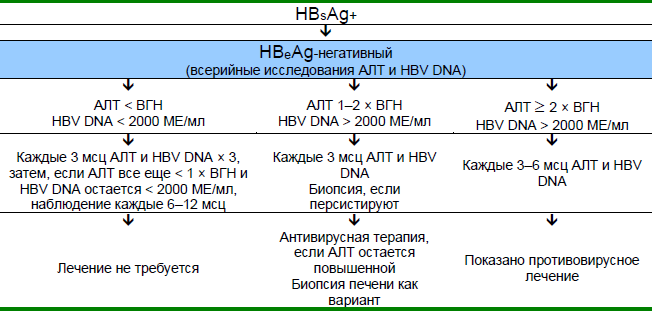
NB: Наблюдение за развитием ГЦК выполняется по показаниям (в зависимости от возраста, пола, тяжести поражения печени и семейного анамнеза).
Верхняя граница нормы (ВГН) АЛТ - 20 МЕ/л у женщин и 30 МЕ/л у мужчин.
Мониторирование HBV DNA каждые 3 месяца у пациентов с АЛТ в один – два раза превышающей верхнюю границу нормы – дорогостоящая процедура и может являться непрактичной в условиях ограниченных ресурсов — см. Каскады ниже и альтернативные подходы.
4.1 Каскады для ведения ХГВ — подход в зависимости от ресурсов
Стандартный подход возможен только при доступности полного спектра диагностических методов и вариантов медикаментозного лечения. Такие ресурсы могут быть доступны не во всех регионах мира. Всемирная Гастроэнтерологическая Организация с помощью своих Каскадов для диагностики и лечению предоставляет подход в зависимости от ресурсов.
- Оценка базового уровня HBV DNA, HDV и ВИЧ рекомендуются при всех ресурсах перед началом любого лечения.
- Первичная оценка ГЦК с помощью ультразвукового исследования должна проводиться во всех случаях, там, где это возможно. В областях с ограниченными ресурсами, высокой эндемичностью, плохой диагностикой ГЦК и ограниченной доступностью высококачественного ультразвука, свою роль в мониторировании все еще играет определение альфа фетопротеина.
Каскад 2 Наблюдение за фазой иммунотолерантности (без лечения)

Каскад 3 Наблюдение за фазой иммуноактивности (после терапии)
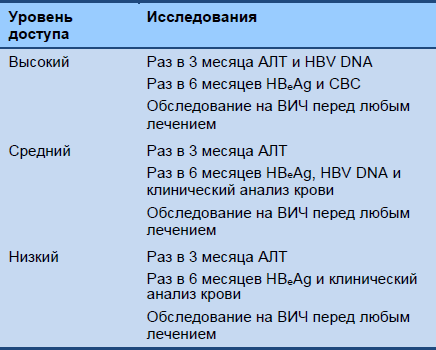
Каскад 4 Наблюдение за фазой иммунного контроля, HBeAg-негативные (после лечения)

Каскад 5 Наблюдение за фазой реактивации, HBeAg-негативные (после лечения)
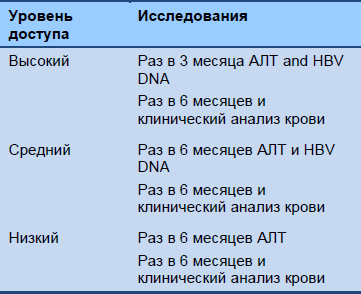
Каскад 6 Наблюдение за иммунореактивной фазой, HBeAg-позитивные

* Титр HBsAg на неделе 12—“правило остановки интерферонотерапии на неделе12”.
Каскад 7 Наблюдение за иммуноактивной фазой, HBeAg-позитивные (АН-терапия)

* Для всех уровней: если пациент получает тенофовир, частота исследования креатинина – в зависимости от функции почек.
** Исследование фосфата требуется только при терапии тенофовиром.
Каскад 8 Наблюдение за фазой реактивации, HBeAg-негативные (АН-терапия)

* Если пациент получает тенофовир, частота исследования креатинина зависит от функции почек.
** Исследование фосфата требуется только при терапии тенофовиром.
4.2 Лечение ХГВ
Одобренные препараты
Таблица 6 Препараты, одобренные для лечения хронического гепатита В
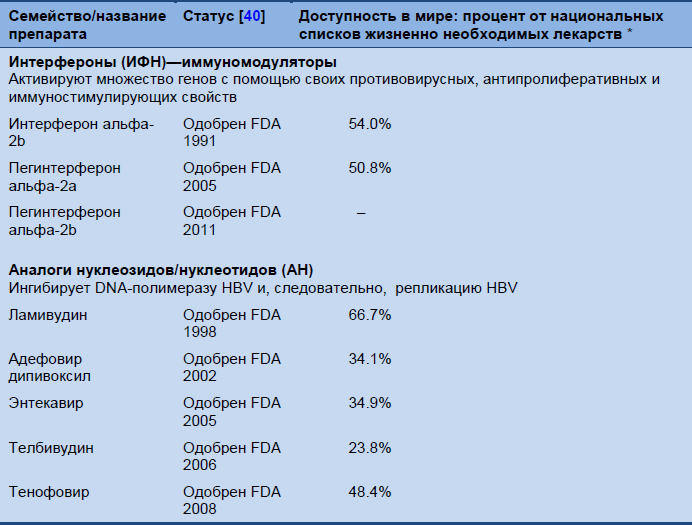
* Сообщенный процент государств-членов ВОЗ по препаратам для гепатита В в их списках жизненно необходимых лекарств или лекарств, субсидируемых правительством [41].
Таблица 7 показывает результаты крупных исследований по лечению HBeAg- негативного и HBeAg-позитивного хронического гепатита В через 6 месяцев после завершения 12-месячного (48 недель) курса пегилированного интерферона альфа (Пег-ИФН) и после 12-месячного (48 или 532 недели) курса терапии аналогами нуклеозидов/нуклеотидов.
Таблица 7 Результаты исследований по лечению HBeAg-негативного и HBeAg-позитивного хронического гепатита В
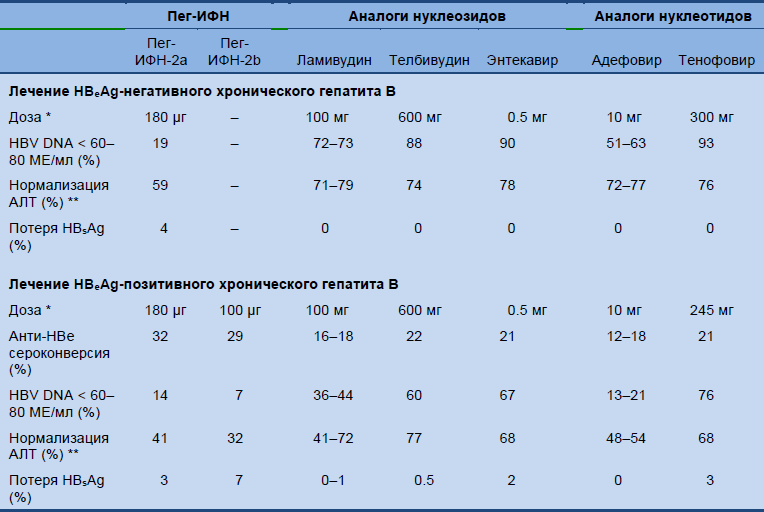
АЛТ, аланин аминотрансфераза; HBV, вирус гепатита В; HBsAg, поверхностный антиген гепатита В; Пег-ИФН, пегинтерферон. Адаптировано из практических рекомендаций EASL 2012 [2]; для последующих ссылок необходимо консультироваться с источником.
* Применение Пег-ИФН: подкожная инъекция 1 раз в неделю; аналогов нуклеозидов/нуклеотидов: оральные таблетки 1 раз в день. ** Определение нормализации АЛТ варьирует в различных исследованиях (например, от снижения АЛТ 1.25 верхней границы нормы (ВГН) в исследовании по энтекавиру до 1.3 ВГН в исследовании по телбивудину).
Для детального обсуждения «золотого стандарта» лечения ХГВ рекомендуется обратиться к последним практическим рекомендациям EASL от 2012 г. [2] (www.easl.eu).
Лекарственная резистентность
При отсутствии ответа или при вирусологическом прорыве, который описывается как повышение уровня HBV DNA до более чем 1 log10 МЕ/мл по сравнению с надиром (самым низким показателем) этого уровня во время лечения с подтвержденным согласием, показана замена, или добавление, на другой препарат с оптимальным профилем резистентности, например, тенофовир или энтекавир.
Для предотвращения развития резистентности могут быть использованы следующие стратегии:
- Для первой линии терапии выбирается мощный противовирусный препарат и/или препарат с низкой частотой резистентности (высокий генетический барьер) в течение длительного времени (энтекавир/тенофовир).
- Еще раз подчеркнуть пациенту важность абсолютного согласия на проведение терапии.
- При использовании препаратов с низкой частотой развития резистентности должно проводиться частое мониторирование уровня HBV DNA level (каждые 3 – 6 месяцев) и исследование резистентности (генотипирование) на случай вирусологического прорыва или субоптимальной вирусной супрессии, для возможности выявления генотипической резистентности до развития клинических последствий.
- Лекарственная резистентность к интерферону описана не была, хотя у некоторых лиц отмечалось отсутствие ответа на лечение, которое в данной ситуации должно быть прекращено. Для контроля над интерферонотерапией может использоваться проведение титра HBsAg, если это доступно (см. ниже).
HBeAg-позитивный гепатит
Рекомендации. HBeAg-позитивные пациенты с персистирующим повышением АЛТ ≥ 2 × верхней границы нормы, и с HBV DNA ≥ 2000 МЕ/мл, должны рассматриваться как кандидаты на лечение.
- Перед началом лечения очень важно провести проверку на наличие ко- инфекции ВИЧ, так как все одобренные аналоги нуклеозидов/нуклеотидов активны против ВИЧ и быстро приводят к развитию лекарственной резистентности вируса, если используются в качестве монотерапии.
- В странах с высокой частотой распространения инфекции вируса гепатита D (Румыния, Молдова, бывшие советские среднеазиатские республики, Россия) обязательно проведение исследований на его наличие.
- Среди пациентов с проведенной биопсией печени лечение в первую очередь назначается тем лицам, у которых определяется умеренное и тяжелое воспаление или выраженный фиброз (≥ F2).
- Лечение должно назначаться больным с циррозом и определяемой HBV DNA, даже при ее низком уровне, вне зависимости от уровня АЛТ.
- Может быть избран любой из одобренных вариантов терапии. Решение зависит от оценки эффективности, безопасности и генетических барьеров резистентности. При АН-терапии предпочтительно назначать энтекавир и тенофовир для того чтобы избежать развития резистентности. Прежде чем начать лечение, важно убедиться, что пациенты имеют достаточные финансовые возможности для приобретения препаратов в течение длительного срока, во избежание резкого прекращения терапии, которое может быть опасным.
- Пациенты должны регулярно наблюдаться с 3-6-месячными интервалами, или чаще при интерферонотерапии, для оценки эффективности, безопасности и развития ранних признаков резистентности (для аналогов нуклеозидов/нуклеотидов).
- В идеале, у пациентов нужно наблюдать за показателями АЛТ, HBeAg, анти-HBe и HBV DNA, но это может оказаться невозможным в странах, где эти исследования недоступны или очень дороги. В такой ситуации достаточно проведения анализа на АЛТ.
- Вирусологический прорыв: повышение уровня HBV DNA > 1 log выше надира после вирусологического ответа, достигнутого на постоянной терапии (для аналогов нуклеозидов/нуклеотидов). Прежде чем предположить появление резистентности необходимо обсудить с пациентом его приверженность терапии. Продолжающееся повышение титров HBV DNA в течение времени позволяет предположить резистентность у пациента, соблюдающего условия лечения.
- У пациентов с резистентностью должен рассматриваться вопрос о назначении «спасательной» терапии нуклеозидами/нуклеотидами, которые не имею профиля перекрестной резистентности (ламивудин, телбивудин и энтекавир имеют наслаивающиеся профили резистентности, поэтому предпочтительна замена на тенофовир – или, если это недоступно, добавление к терапии адефовира).
- Прием оральных препаратов должен продолжаться минимум 12 месяцев после конечной точки сероконверсии HBeAg при HBeAg-позитивном гепатите, и его предпочтительно продолжать до возникновения потери HBsAg из-за высокого риска реактивации после прекращения терапии. После остановки или отмены оральной терапии рекомендуется проводить тщательное наблюдение из-за риска обострения заболевания после прекращения лечения.
- Преимущество терапии пегинтерфероном заключается в фиксированной длительности курса лечения. Сероконверсия HBeAg может произойти в срок до 6 месяцев после прекращения интерферонотерапии. Потеря HBeAg и сероконверсия, вызванные интерфероном, представляются более надежными, по сравнению с аналогами нуклеозидов/нуклеотидов. Интерферон наиболее эффективен при генотипе А инфекции, и менее эффективен при генотипах D и C.
- Если доступно исследование титров HBsAg, то они могут помочь в коррекции интерферонотерапии. Прекращение интерферонотерапии показано всем пациентам с HBsAg > 20,000 МЕ/мл на неделе 24, вне зависимости от генотипа HBV [42]. Альтернативно, пациенты без снижения титра HBsAg на неделе 12, также должны прекратить терапию. Правила прекращения улучшают показатель стоимости-эффективности при терапии интерфероном [43].
HBeAg-негативный гепатит
HBeAg-негативный ХГВ представляет собой позднюю стадию течения хронической инфекции HBV.
- Пациент должен рассматриваться как кандидат на терапию, если:
- HBV DNA ≥ 20,000 МЕ/мл и сывороточная АЛТ > 2 × ВГН
- Биопсия печени или другие методы оценки фиброза должны рассматриваться у пациентов, если:
- HBV DNA ≥ 20,000 МЕ/мл и сывороточная АЛТ < 2 × ВГН
- HBV DNA ≥ 2000 МЕ/мл и/или сывороточная АЛТ > ВГН
- Лечение должно быть назначено, если при биопсии печени имеется умеренное/тяжелое некровоспаление или выраженный фиброз (≥ F2)
- Лечение любого пациента с циррозом и определяемой HBV DNA.
Рекомендации для лечения:
- Перед началом лечения очень важно провести проверку на наличие ко- инфекции ВИЧ, так как все одобренные аналоги нуклеозидов/нуклеотидов активны против ВИЧ и быстро приводят к развитию лекарственной резистентности вируса, если используются в качестве монотерапии.
- Лечение может проводиться традиционным интерфероном, пегинтерфероном альфа или аналогами нуклеозидов/нуклеотидов. При печеночной недостаточности интерферонотерапия проводится не должна.
- Пациентам с противопоказаниями к интерферону, такими как декомпенсированный цирроз или аутоиммунное заболевание, рекомендуется лечение аналогами нуклеозидов/нуклеотидов.
- Длительность терапии интерфероном или пегинтерфероном составляет 1 год. Если к 12-й неделе HBsAg не снизился, в сочетании с уменьшением менее 2 log HBV DNA, интерферонотерапия должна быть прекращена, поскольку ответ уже маловероятен [42,44].
- Для оральной терапии, особенно пациентам с циррозом, предпочтительно назначать препараты с низкой резистентностью, такие как энтекавир или тенофовир. Тем не менее, там где роль играют экономические ограничения, терапия может начинаться с ламивудина (или телбивудина), с ранним добавлением адефовира или переходом на тенофовир, при развитии лекарственной резистентности, или при сохранении уровня HBV DNA ≥ 2000 МЕ/мл на 24-й неделе лечения.
- Оптимальная длительность противовирусной терапии при HBeAg- негативном ХГВ неизвестна, но она должна быть долговременной, возможно пожизненной, или продолжаться до потери HBsAg, как минимум.
- Рекомендуется наблюдение за биохимическими показателями и HBV DNA каждые 3 – 6 месяцев для оценки ответа на лечение и раннего выявления лекарственной резистентности.
- При выявлении лекарственной резистентности должно добавляться лекарство с неперекрывающимся профилем резистентности (адефовир при резистентности к ламивудину).
- При повышенной АЛТ и низком уровне HBV DNA (< 2000 МЕ/мл), должны быть исключены другие причины воспаления (жировая печень, медикаментозное лечение, ко-инфекция HDV и HCV). HDV ингибирует репликацию HBV, и, следовательно, ко-инфицированные HDV пациенты обычно HBeAg-негативны, с низким или даже неопределяемым уровнем HBV DNA, но с постоянно повышенной АЛТ, и часто с признаками выраженного фиброза/цирроза.
4.3 Ко-инфекция
HBV–HDV
Вирус гепатита D - (HDV) – это дефектный вирус с круговым геномом РНК и единственным структурированным белком, антигеном гепатита дельта. Вирусу требуется поверхностный антиген HBV, который служит оболочкой для его дельта антигена. Такая вспомогательная функция HBV необходима для сборки и размножения HDV.
- До 5% мировой популяции инфицировано HBV, и, вероятно, 5% из хронически инфицированных HBV имеют инфекцию HDV.
- Тем не менее, в некоторых эндемичных областях наблюдаются более высокие показатели распространенности (Африканский Рог, Восточная Европа, бассейн Амазонки). Вирус ко-инфицирует одновременно с HBV, или суперинфицирует у лиц уже хронически инфицированных HBV.
- Ко-инфекция переходит в хроническую форму только в 2% случаев, но она связана с повышенным риском фульминантной острой инфекции, в то время как суперинфекция приводит к прогрессированию заболевания и циррозу более чем в 80% случаев.
- Цирроз развивается в более молодом возрасте, чем при хронической моноинфекции HBV.
Рекомендации:
- Должна вводиться всеобщая вакцинация против HBV для предотвращения инфекции HDV и, следовательно, ее распространения среди населения.
- HBsAg-позитивные пациенты должны оцениваться на наличие инфекции HDV, особенно если у пациента наблюдается малая или отсутствует репликация HBV (т.е., низкая HBV DNA), или если больные поступают из эндемичного по HDV региона, или были инфицированы HBV при употреблении инъекционных наркотиков.
- Инфекция HDV может быть выявлена посредством определения HDV RNA в сыворотке крови с помощью цепной полимеразной реакции, или непрямым определением антител к антигену гепатита D (анти-HDV) классов IgG и IgM.
- Лечение хронического гепатита D должно проводиться интерфероном (предпочтительно пегилированным интерфероном) минимум 12 месяцев, но результаты его субоптимальны. Эффективным для пациентов с активной репликацией HBV, несмотря на ко-инфекцию HDV, может оказаться терапия аналогами нуклеозидов/нуклеотидов (АН) в комбинации с пегинтерфероном.
HBV–HCV
Ко-инфекция HBV и вирусом гепатита С (HCV) возможна, поскольку обе имеют сходные факторы риска и некоторые общие пути передачи. Ко-инфекция наиболее часто встречается в регионах высоко эндемичных для обоих вирусов и у лиц, имевших контакт с инфекцией через зараженные иглы при использовании инъекционных наркотиков — так как, в отличие от HBV, HCV редко передается половым или вертикальным путем. По тем же самым причинам, ко-инфекция HBV и HCV — и даже тройная инфекция HBV, HCV и ВИЧ, а потенциально и четверная инфекция (с HDV в дополнение) — может наблюдаться в группах повышенного риска.
- Интерфероны (и пегилированные интерфероны) – это хорошо известные терапевтические агенты против HBV и HCV, являющиеся терапией выбора для ко-инфицированных пациентов (при отсутствии ВИЧ).
- При доминировании HCV (с определяемой HCV RNA и низкой или неопределяемой HBV DNA), приоритетным должно стать лечение HCV, который быстро прогрессирует. Предпочтительна интерферонотерапия HCV для одновременного контроля HBV, но исчерпывающих данных по этому подходу в настоящее время нет. Новые безинтерфероновые методы лечения HCV высокоэффективны и их применение должно рассматривается у пациентов с ко-инфекцией HBV/HCV. Сейчас оценивается оптимальный подход для данной популяции больных.
- При доминировании HBV (с высоким уровнем HBV DNA), гепатит C часто подавляется (т.е., HCV-RNA не определяется). В таких случаях, решение о лечении HBV принимается вне зависимости от наличия инфекции HCV в прошлом.
- Требуется регулярное наблюдение за уровнем АЛТ, HCV RNA и HBV DNA во время и после терапии, поскольку подавление доминирующего вируса с помощью противовирусной терапии может вызвать реактивацию вируса, подавленного ранее.
HBV–ВИЧ
Примерно 36 миллионов человек по всему миру инфицированы ВИЧ. Может иметь место хроническая ко-инфекция HBV, так как передача вирусов происходит общими путями — парентеральным, вертикальным и половым.
- Распространенность ХГВ среди ВИЧ-инфицированных больных может в десять и более раз превышать данные для общей популяции.
- Хроническая инфекция HBV встречается у 5–10% ВИЧ-инфицированных лиц в Западной Европе и Соединенных Штатах [45]
- Прогрессирование ХГВ в цирроз, заболевание печени конечной стадии, и/или ГЦК происходит у ВИЧ-инфицированных пациентов быстрее, чем у больных только с ХГВ [46].
Отсутствие контролируемых исследований и двойная активность некоторых препаратов осложняют ведение инфекции ХГВ у пациентов с ко-инфекцией ВИЧ. Схемы лечения зависят от клинического статуса как ВИЧ, так и HBV.
- Многие одобренные аналоги нуклеозидов/нуклеотидов, активные против HBV, также подавляют ВИЧ, следовательно, очень важно избегать монотерапии любым одобренным оральным препаратом против HBV, в связи с быстрым развитием резистентности ВИЧ и, возможно, HBV. При показаниях к лечению, предпочтение отдается тенофовиру в комбинации с другими высоко активными в отношении ВИЧ препаратами.
- Таким образом, все пациенты с ХГВ всегда должны обследоваться на наличие ко-инфекции ВИЧ перед началом противовирусного лечения.
Принципиальными целями лечения инфекции HBV являются остановка или уменьшение прогрессирования заболевания печени и предотвращение развития цирроза и ГЦК.
- Пролонгированное подавление репликации HBV приводит к гистологическому улучшению, значительному снижению или нормализации уровней аминотрансфераз и предотвращению прогрессирования в цирроз и терминальную стадию заболевания.
- Устойчивый вирусный контроль требует проведения длительной поддерживающей терапии.
- Прекращение лечения в частности может быть связано с реактивацией HBV и повышением уровня АЛТ.
- Недостаточность длительной терапии – это риск развития резистентности HBV. Для снижения лекарственной резистентности большинству пациентов с ко-инфекцией требуется комбинированное лечение HBV.
4.4 Беременность
Ниже следующие рекомендации также основаны на практических рекомендациях EASL 2012 [2]:
- Все беременные женщины должны быть обследованы на HBsAg.
- Перед началом лечения ХГВ должен обсуждаться риск для плода в случае беременности и для планирования семьи пациентки.
- (Пег-)ИФН противопоказан во время беременности.
- Тенофовир имеет лучший профиль резистентности и более расширенные данные по безопасности при беременности у женщин с ХГВ по сравнению с телбивудином (оба препарата входят в категорию В для беременности: нет риска в испытаниях на животных, риск при применении у человека неизвестен) [47]. Данные по ВИЧ-положительным беременным женщинам позволяют предположить, что применение ламивудина, эмтрицитабина и тенофовира безопасно [48,49].
- Перинатальное заражение ВИЧ в основном происходит в момент родов, и профилактика фокусируется на пассивной и активной иммунизации иммуноглобулином гепатита В (HBIg) и вакцинации от HBV, которые должны проводиться в срок 12 часов после рождения.
- В мета-анализе пользы назначения HBIg новорожденным для профилактики передачи инфекции HBV от матери к ребенку (ПМР), показано, что HBIg и плазменная вакцина от HBV уменьшали количество заражений с 20% до 10% по сравнению с моноприменением вакцины (ОР 0.49; 95% ДИ, 0.32 to 0.74); при применении HBIg и рекомбинантной HBV вакцины трансмиссия снижалась от 30.8% до 18.9% (ОР 0.61; 95% ДИ, 0.41 до 0.92) [50].
- Женщины с высокой концентрацией HBV DNA (сывороточная HBV DNA > 106–7 МЕ/мл, и в основном HBeAg-позитивные) все равно могут иметь повышенный риск ПМР несмотря на соответствующую вакцинацию, поэтому они должны рассматриваться как кандидаты на лечение ламивудином, телбивудином или тенофовиром в течение последнего триместра беременности, в дополнение к пассивной и активной вакцинации HBIg и HBV вакцинации.
- В мета-анализе РКИ, ламивудин снижал число заражений HBV с 25.4% до 12% по сравнению с плацебо при назначении в последнем триместре беременности. По сравнению с пациентками, получавшими HBIg, ламивудин уменьшал трансмиссию с 20.4% до 6.3% [51]. В мета-анализе терапии телбивудином при беременности, обобщенные результаты были сходными с результатами по ламивудину, но анализ включал только два РКИ и три не-РКИ [52].
- АН-терапия назначаемая только для профилактики перинатального заражения, может быть прекращена в течение первых 3 месяцев после родов.
- За женщинами с ХГВ необходимо тщательное наблюдение после родов из-за возможности развития обострения [53].
5. Вакцинация против гепатита В
Программа всеобщей вакцинации новорожденных – это важнейший шаг к эффективному контролю над инфекцией HBV во всем мире. Вакцинация против HBV показала высокие показатели стоимости-эффективности. Вакцинация предотвращает развитие инфекции и, таким образом, уменьшает частоту хронического гепатита, цирроза и ГЦК в вакцинированной популяции, а также снижает возможность передачи инфекции, ограничивая круг восприимчивых к ней лиц.
5.1 Активная вакцинация против гепатита В
HBsAg – это антиген, используемый в составлении вакцины против гепатита В. Она производится из дрожжей с использованием технологии рекомбинантных ДНК. Доступна как моносостав, или фиксированная комбинация с другими вакцинами.
5.2 Пассивная вакцинация иммуноглобулином гепатита В
Иммуноглобулин гепатита В (HBIg) приготовляется из плазмы лиц с высокой концентрацией анти-HB. Стандартная доза HBIg составляет 0.06 мл/кг для любого применения у взрослых или 200 МЕ у новорожденных. В стандартных дозах он обеспечивает временную (т.е., приблизительно на 3 – 6 месяцев) защиту от инфекции HBV. HBIg вводится внутримышечно, предпочтительно в дельтовидную или ягодичную мышцу. При одновременном применении с вакциной против гепатита В, HBIg вводится в другую инъекционную область.
5.3 Первичная профилактика
Современная стратегия элиминации передач ХГВ должна начинаться с программы первичной профилактики. Она должна включать:
- Всеобщую вакцинацию всех новорожденных; обязательную для новорожденных от матерей с позитивным поверхностным антигеном гепатита В.
- Вторичную профилактику для детей, у чьих матерей неизвестно состояние HBsAg.
- «Догоняющую» вакцинацию для ранее не привитых детей и подростков.
- Вакцинацию не привитых взрослых, подверженных риску инфекции HBV (тем не менее, обычно лица «высокого риска» не имеют доступа к медицинской помощи или не информированы о возможностях медучреждений; отсюда необходимость всеобщей вакцинации новорожденных).
- Вакцинация лиц с наиболее высоким риском развития тяжелой инфекции – например, пациентов с хроническим заболеванием печени.
5.4 Схемы вакцинации
Комбинация распространенности, пути передачи и вирусных факторов имеет значение для стратегии — вакцинация групп риска, вакцинация новорожденных или подростковая вакцинация.
Вакцина у взрослых вводится внутримышечно в дельтовидную мышцу (не в ягодичную), или в переднелатеральную область бедра у новорожденных.
- Проведенные исследования позволяют предположить, что всеобщая вакцинация стоимостно-эффективна в странах с высокой или средней степенью распространения инфекции.
- В Европе и Северной Америке, где частота заболевания очень мала, применяется либо рутинная детская вакцинация, либо вакцинация новорожденных, у чьих матерей определяется поверхностный антиген гепатита В (HBsAg).
- Рутинная вакцинация подростков в возрасте 10 лет и «догоняющая» вакцинация для взрослых из группы риска (идентифицировать и/или получить доступ к таким лицам сложно) рекомендованы в некоторых странах, но имеют мало влияния на частоту хронической инфекции.
Рекомендации по вакцинации:
- Первичная вакцинация, состоящая из трех внутримышечных инъекций вакцины гепатита В, проводится в возрасте 0.1 и 6 месяцев, приводит к позитивному ответу антител у 30–55% взрослых в возрасте ≤ 40 years после первой дозы, у 75% после второй дозы, и у > 90% после третьей дозы. Такие уровни ответа снижаются, когда вакцинация проводится пожилым людям (например, < 90% у лиц > 40 лет, 75% у лиц старше 60 лет).
- Другие инновационные схемы вакцинации (например, в 0, 1 и 4 месяца или в 0, 2 и 4 месяца или в 0, 1 и 2 месяца) способны вызывать дозо специфичные и окончательные результаты, сходные с полученными при схеме 0.1 – 6 месяцев, и могут оказаться более практичными для новорожденных.
- Ускоренные схемы вакцинации для вторичной профилактики у взрослых часто обеспечивают получение согласия на завершение схемы вакцинации.
- Дети, рожденные от HBsAg-позитивных матерей, должны получать первую дозу вакцины в течение 12 часов после рождения.
- Известно, что факторы хозяина (например, курение, ожирение, цирроз, генетические факторы, иммуносупрессия, почечная недостаточность и т.д.) приводят к снижению ответа на вакцинацию.
- Лица, не достигшие анти-HBs ответа (≥ 10 mМЕ/мл) при схеме первичной вакцинации, должны получить повторную трехдозовую вакцинацию (через 0, 1 и 2 месяца). Это повышает защитный уровень антител у 44–100% людей. Лица, у которых не развился защитный уровень анти-HBs после ревакцинации, должны рассматриваться как кандидаты на повторную вакцинацию (0, 1 и 2 месяца с усилением вакцинации через 6 месяцев) двойной стандартной дозой вакцины.
- Для лиц ≥ 18 лет, не проживающих в эндемичных по гепатиту А областях, доступна комбинированная вакцина против гепатита А и В (Twinrix).
5.5 Вторичная вакцинация
Вторичная вакцинация, если она может быть проведена вовремя, должна рассматриваться для лиц, имевших контакт (парентеральный или половой) с кровью или другими жидкостями тела.
- До введения вакцины должна быть проведена оценка статуса HBsAg источника инфекции и анти-HBs статуса контактировавшего человека.
- Также, оценка наличия HBsAg должна проводиться в странах с высоким уровнем эндемичности HBV.
- Ранее не привитые лица получают и HBIg и вакцину против гепатита В сразу после контакта (желательно в течение 24 часов). Вакцина против гепатита В вводится одновременно с HBIg в различные места для инъекций.
- Завершение вакцинации против гепатита В происходит в те же сроки – в 0, 1 и 6 месяцев или в 0, 1 и 2 месяца.
Контактировавший человек, находящийся в процессе вакцинации (но еще не завершивший серию) должен получить соответствующую дозу HBIg с рекомендациями завершения серии вакцинации против гепатита В.
Ответившие на введение вакцины лица могут удерживать защитный уровень анти-HBs в течение различного времени. Люди, прошедшие вакцинацию защищены, как минимум, на 20 лет (возможно, пожизненно), даже если у них отсутствовал определяемый уровень анти-HBs на момент контакта. У ответивших на введение вакцины может возникнуть бессимптомная острая инфекция гепатита В вслед за снижением уровня анти-HBs, она обычно саморазрешается. У некоторых вакцинированных пациентов выявлялась оккультная инфекция гепатита В, но клиническое значение этого пока не ясно [54].
Таким образом, иммунокомпетентные лица, ответившие на вакцинацию против гепатита В концентрацией анти-HBs ≥ 10 mМЕ/мл, не требуют дополнительной пассивной или активной иммунизации после контакта с HBV. В дополнение к этому, они не нуждаются в дальнейшем периодическом исследовании концентрации анти-HBs. Тем не менее, если предыдущая концентрация анти-HBs не известна (не исследовалась рутинно), или составляет < 10 mМЕ/мл, необходимо назначение HBIg и вакцины. Если контактировавший человек известен как неответивший, могут быть назначены две дозы HBIg, с интервалом в 1 месяц.
Усиливающие дозы не рекомендованы для рутинного применения у иммунокомпетентных лиц, когда бы они ни вакцинировались – при рождении, в подростковом возрасте, или взрослыми. Подобно этому, не рекомендуется проведение серологических исследований для оценки уровня антител в любой возрастной группе, за исключением, возможно, лиц с высоким риском заражения, таким как бытовые контакты с инфицированными людьми или работа в здравоохранении – т.е. усиливающая доза должна вводиться при уровне анти-HBs < 10 mМЕ/мл. Очень важно рекомендовать усиливающую дозу лицам с явным, продолжающимся контактом с инфекцией HBV (т.е., когда сексуальный партнер HBsAg-позитивен, или человек работает в медицинском учреждении).
5.6 Беременность и вакцинация против гепатита В
При введении вакцины против гепатита В беременным женщинам нет тератогенного или любого другого риска. Не существует противопоказаний для введения вакцины беременным женщинам или кормящим матерям.
6. Приложение
6.1 Сокращения
|
AASLD
|
Американская Ассоциация по Изучению Болезней Печени
|
|
АФП
|
Альфа фетопротеин
|
|
АЛТ
|
Аланин аминотрансфераза
|
|
АСТ
|
Аспартат аминотрансфераза
|
|
APASL
|
Азиатско-Тихоокеанская Ассоциация по Изучению Печени
|
|
ОКП
|
Основной коровый промотор
|
|
ХГВ
|
Хронический гепатит В
|
|
ДИ
|
Доверительный интервал
|
|
EASL
|
Европейская Ассоциация по Изучению Печени
|
|
FDA
|
Администрация США по пищевым продуктам и лекарственным препаратам
|
|
HBc
|
Кор (антиген) гепатита В
|
|
HBeAg
|
е антиген гепатита В
|
|
HBIg
|
Иммуноглобулин гепатита В
|
|
HBsAg
|
Поверхностный антиген гепатита В
|
|
HBV
|
Вирус гепатита В
|
|
ГЦК
|
Гепатоцеллюлярная карцинома
|
|
HCV
|
Вирус гепатита С
|
|
HDV
|
Вирус гепатита D
|
|
ВИЧ
|
Вирус иммунодефицита человека
|
|
ИФН
|
Интерферон
|
|
IgG
|
Иммуноглобулин G
|
|
IgM
|
Иммуноглобулин M
|
|
МНО
|
Международное нормализованное отношение
|
|
МЕ/мл
|
Международные единицы на миллилитр (стандарт ВОЗ для концентраций HBV DNA)
|
|
ПМР
|
Передача от матери ребенку
|
|
АН
|
Аналог нуклеозидов
|
|
НАЖБП
|
Неалкогольная жировая болезнь печени
|
|
НАСГ
|
Неалкогольный стеатогепатит
|
|
NICE
|
Национальный Институт Помощи и Медицинского Мастерства
|
|
НПВП
|
Нестероидные противовоспалительные препараты
|
|
ПЦР
|
Полимеразная цепная реакция
|
|
Пег-ИФН
|
Пегинтерферон
|
|
РКИ
|
Рандомизированное контролируемое исследование
|
|
ОР
|
Относительный риск
|
|
СКС
|
Системные кортикостероиды
|
|
ВГН
|
Верхняя граница нормы
|
|
ВГО
|
Всемирная гастроэнтерологическая Организация
|
|
ВОЗ
|
Всемирная Организация Здравоохранения
|
Определения часто используемых терминов можно найти на странице 533 практических рекомендаций APASL 2012 [4].
6.2 References
- Lok ASF, McMahon BJ. Chronic hepatitis B: update 2009. Hepatology 2009;50:661–2.
- European Association for the Study of the Liver. EASL clinical practice guidelines: management of chronic hepatitis B virus infection. J Hepatol 2012;57:167–85.
- National Institute for Health and Care Excellence (NICE). Hepatitis B (chronic): diagnosis and management of chronic hepatitis B in children, young people and adults [Internet]. London: NICE; 2013. Available from: http://www.nice.org.uk/guidance/cg165/resources/guidance-hepatitis-b-chronic-pdf
- Liaw YF, Kao JH, Piratvisuth T, Chan HLY, Chien RN, Liu CJ, et al. Asian–Pacific consensus statement on the management of chronic hepatitis B: a 2012 update. Hepatol Int 2012;6:531–61.
- World Health Organization. Global Alert and Response (GAR): Hepatitis [Internet]. Geneva: World Health Organization [cited 2015 Mar 31]. Available from: http://www.who.int/csr/disease/hepatitis/en/.
- Ott JJ, Stevens GA, Groeger J, Wiersma ST. Global epidemiology of hepatitis B virus infection: new estimates of age-specific HBsAg seroprevalence and endemicity. Vaccine 2012;30:2212–9.
- Hepatitis B Foundation. Hepatitis B Foundation [Internet]. Doylestown, PA. Available from: http://www.hepb.org/.
- Lozano R, Naghavi M, Foreman K, Lim S, Shibuya K, Aboyans V, et al. Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet 2012;380:2095–128.
- Hollinger F, Liang T. Hepatitis B virus. In: Knipe DM, Howley PM, editors. Fields’ virology. 4th ed. Philadelphia: Lippincott Williams & Wilkins; 2001. p. 2971–3036.
- Sunbul M. Hepatitis B virus genotypes: global distribution and clinical importance. World J Gastroenterol 2014;20:5427.
- Shi W, Zhang Z, Ling C, Zheng W, Zhu C, Carr MJ, et al. Hepatitis B virus subgenotyping: history, effects of recombination, misclassifications, and corrections. Infect Genet Evol 2013;16:355–61.
- Chulanov V, Neverov A, Karandashova I, Dolgin V, Mikhailovskaya G, Lebedeva E, et al. Molecular epidemiology of HBV in Russia [abstract C.222]. Abstracts of the 14th International Symposium on Viral Hepatitis and Liver Disease. China, Shanghai, 2012.
- Deterding K, Constantinescu I, Nedelcu FD, Gervain J, Nemecek V, Srtunecky O, et al. Prevalence of HBV genotypes in Central and Eastern Europe. J Med Virol 2008;80:1707–11.
- Devesa M, Loureiro CL, Rivas Y, Monsalve F, Cardona N, Duarte MC, et al. Subgenotype diversity of hepatitis B virus American genotype F in Amerindians from Venezuela and the general population of Colombia. J Med Virol 2008;80:20–6.
- Blitz L, Pujol FH, Swenson PD, Porto L, Atencio R, Araujo M, et al. Antigenic diversity of hepatitis B virus strains of genotype F in Amerindians and other population groups from Venezuela. J Clin Microbiol 1998;36:648–51.
- Cardona NE, Loureiro CL, Garzaro DJ, Duarte MC, García DM, Pacheco MC, et al. Unusual presentation of hepatitis B serological markers in an Amerindian community of Venezuela with a majority of occult cases. Virol J 2011;8:527.
- Pujol FH, Navas MC, Hainaut P, Chemin I. Worldwide genetic diversity of HBV genotypes and risk of hepatocellular carcinoma. Cancer Lett 2009;286:80–8.
- Kramvis A, Kew M, François G. Hepatitis B virus genotypes. Vaccine 2005;23:2409–23.
- Kimbi GC, Kramvis A, Kew MC. Distinctive sequence characteristics of subgenotype A1 isolates of hepatitis B virus from South Africa. J Gen Virol 2004;85:1211–20.
- Kramvis A, Kew MC. Epidemiology of hepatitis B virus in Africa, its genotypes and clinical associations of genotypes. Hepatol Res 2007;37(s1):S9–S19.
- Yousif M, Mudawi H, Bakhiet S, Glebe D, Kramvis A. Molecular characterization of hepatitis B virus in liver disease patients and asymptomatic carriers of the virus in Sudan. BMC Infect Dis 2013;13:328.
- Devesa M, Pujol FH. Hepatitis B virus genetic diversity in Latin America. Virus Res 2007;127:177–84.
- Ahmed CS, Wang Z, Bin Z, Chen J, Kamal M, Hou J. Hepatitis B virus genotypes, subgenotypes, precore, and basal core promoter mutations in the two largest provinces of Pakistan. J Gastroenterol Hepatol 2009;24:569–73.
- De Franchis R, Hadengue A, Lau G, Lavanchy D, Lok A, McIntyre N, et al. EASL International Consensus Conference on Hepatitis B. 13–14 September, 2002 Geneva, Switzerland. Consensus statement (long version). J Hepatol 2003;39 Suppl 1:S3–25.
- 2McMahon BJ. Epidemiology and natural history of hepatitis B. Semin Liver Dis 2005;25 Suppl 1:3–8.
- World Health Organization. Hepatitis B. WHO fact sheet no. 204 [Internet]. Geneva: World Health Organization; 2015. Available from: http://www.who.int/mediacentre/factsheets/fs204/en/.
- Santantonio T, Fasano M. Current concepts on management of chronic hepatitis B. In: Serviddio G, editor. Practical management of chronic viral hepatitis [Internet]. InTech; 2013 [cited 2015 Mar 31]. Available from: http://www.intechopen.com/books/practical-management-of-chronic-viral-hepatitis/current-concepts-on-management-of-chronic-hepatitis-b.
- Hui CK, Leung N, Yuen ST, Zhang HY, Leung KW, Lu L, et al. Natural history and disease progression in Chinese chronic hepatitis B patients in immune-tolerant phase. Hepatology 2007;46:395–401.
- Brunetto MR, Oliveri F, Colombatto P, Moriconi F, Ciccorossi P, Coco B, et al. Hepatitis B surface antigen serum levels help to distinguish active from inactive hepatitis B virus genotype D carriers. Gastroenterology 2010;139:483–90.
- Raimondo G, Allain JP, Brunetto MR, Buendia MA, Chen DS, Colombo M, et al. Statements from the Taormina expert meeting on occult hepatitis B virus infection. J Hepatol 2008;49:652–7.
- Zerbini A, Pilli M, Boni C, Fisicaro P, Penna A, Di Vincenzo P, et al. The characteristics of the cell-mediated immune response identify different profiles of occult hepatitis B virus infection. Gastroenterology 2008;134:1470–81.
- Peng CY, Chien RN, Liaw YF. Hepatitis B virus-related decompensated liver cirrhosis: benefits of antiviral therapy. J Hepatol 2012;57:442–50.
- Fattovich G, Bortolotti F, Donato F. Natural history of chronic hepatitis B: special emphasis on disease progression and prognostic factors. J Hepatol 2008;48:335–52.
- Lee IC, Lin CH, Huang YH, Huo TI, Su CW, Hou MC, et al. IL28B polymorphism correlates with active hepatitis in patients with HBeAg-negative chronic hepatitis B. PloS One 2013;8:e58071.
- Kim TW, Kim MN, Kwon JW, Kim KM, Kim SH, Kim W, et al. Risk of hepatitis B virus reactivation in patients with asthma or chronic obstructive pulmonary disease treated with corticosteroids. Respirology 2010;15:1092–7.
- Huang YH, Hsiao LT, Hong YC, Chiou TJ, Yu YB, Gau JP, et al. Randomized controlled trial of entecavir prophylaxis for rituximab-associated hepatitis B virus reactivation in patients with lymphoma and resolved hepatitis B. J Clin Oncol 2013;31:2765–72.
- Singal AG, Conjeevaram HS, Volk ML, Fu S, Fontana RJ, Askari F, et al. Effectiveness of hepatocellular carcinoma surveillance in patients with cirrhosis. Cancer Epidemiol Biomark Prev 2012;21:793–9.
- Liaw YF, Leung N, Kao JH, Piratvisuth T, Gane E, Han KH, et al. Asian–Pacific consensus statement on the management of chronic hepatitis B: a 2008 update. Hepatol Int 2008;2:263–83.
- Lok ASF, McMahon BJ. Chronic hepatitis B. Hepatology 2007;45:507–39.
- Hepatitis B Foundation. HBF drug watch: compounds in development for chronic hepatitis B. Updated December 15, 2014 [Internet]. Available from: http://www.hepb.org/professionals/hbf_drug_watch.htm
- World Health Organization. Global policy report on the prevention and control of viral hepatitis in WHO member states [Internet]. Geneva: World Health Organization; 2013. Available from: http://www.who.int/hiv/pub/hepatitis/global_report/en/
- Sonneveld MJ, Hansen BE, Piratvisuth T, Jia JD, Zeuzem S, Gane E, et al. Response-guided peginterferon therapy in hepatitis B e antigen-positive chronic hepatitis B using serum hepatitis B surface antigen levels. Hepatology 2013;58:872–80.
- Lo AOS, Wong VWS, Wong GLH, Chan HLY, Dan YY. Cost effectiveness of response-guided therapy with peginterferon in the treatment of chronic hepatitis B. Clin Gastroenterol Hepatol 2015;13:377–85.
- Sonneveld MJ, Rijckborst V, Boucher CAB, Hansen BE, Janssen HLA. Prediction of sustained response to peginterferon alfa-2b for hepatitis B e antigen-positive chronic hepatitis B using on-treatment hepatitis B surface antigen decline. Hepatology 2010;52:1251–7.
- Spradling PR, Richardson JT, Buchacz K, Moorman AC, Brooks JT, HIV Outpatient Study (HOPS) Investigators. Prevalence of chronic hepatitis B virus infection among patients in the HIV Outpatient Study, 1996–2007. J Viral Hepat 2010;17:879–86.
- Thio CL, Seaberg EC, Skolasky R, Phair J, Visscher B, Muñoz A, et al. HIV-1, hepatitis B virus, and risk of liver-related mortality in the Multicenter Cohort Study (MACS). Lancet 2002;360:1921–6.
- Borgia G, Carleo MA, Gaeta GB, Gentile I. Hepatitis B in pregnancy. World J Gastroenterol 2012;18:4677–83.
- Terrault NA, Jacobson IM. Treating chronic hepatitis B infection in patients who are pregnant or are undergoing immunosuppressive chemotherapy. Semin Liver Dis 2007;27 Suppl 1:18–24.
- Chotiyaputta W, Lok AS. Role of antiviral therapy in the prevention of perinatal transmission of hepatitis B virus infection. J Viral Hepat 2009;16:91–3.
- Lee C, Gong Y, Brok J, Boxall EH, Gluud C. Effect of hepatitis B immunisation in newborn infants of mothers positive for hepatitis B surface antigen: systematic review and meta-analysis. BMJ 2006;332:328–36.
- Han L, Zhang HW, Xie JX, Zhang Q, Wang HY, Cao GW. A meta-analysis of lamivudine for interruption of mother-to-child transmission of hepatitis B virus. World J Gastroenterol 2011;17:4321–33.
- Deng M, Zhou X, Gao S, Yang SG, Wang B, Chen HZ, et al. The effects of telbivudine in late pregnancy to prevent intrauterine transmission of the hepatitis B virus: a systematic review and meta-analysis. Virol J 2012;9:185.
- Ter Borg MJ, Leemans WF, de Man RA, Janssen HLA. Exacerbation of chronic hepatitis B infection after delivery. J Viral Hepat 2008;15:37–41.
- Lai MW, Lin TY, Tsao KC, Huang CG, Hsiao MJ, Liang KH, et al. Increased seroprevalence of HBV DNA with mutations in the s gene among individuals greater than 18 years old after complete vaccination. Gastroenterology 2012;143:400–7.


























